Zakażenia układu oddechowego pozostają jednym z najważniejszych obciążeń dla systemu ochrony zdrowia w krajach rozwiniętych. Są odpowiedzialne za znaczną liczbę wizyt ambulatoryjnych, hospitalizacji, powikłań i zgonów, szczególnie wśród niemowląt, małych dzieci, osób starszych oraz pacjentów obciążonych chorobami przewlekłymi. Do patogenów, które w istotny sposób przyczyniają się do tego obciążenia, należą m.in. bakterie gatunku Streptococcus pneumoniae, nazywane pneumokokami, oraz syncytialny wirus oddechowy (RSV). Co więcej, coraz więcej badań wskazuje, że oba patogeny mogą wzajemnie na siebie oddziaływać w sposób pogarszający przebieg choroby u pacjenta.
Artykuł prof. dr hab. n.med i n. o zdr. Piotra Rzymskiego z Zakładu Medycyny Środowiskowej Uniwersytetu Medycznego im. Karola Marcinkowskiego w Poznaniu z numeru 4/2026 Biuletynu Informacyjnego Wielkopolskiej Izby Lekarskiej.
RSV jest jednym z najczęstszych wirusowych czynników zakażeń dolnych dróg oddechowych. U niemowląt i małych dzieci stanowi istotną przyczynę zapalenia w obrębie dolnych dróg oddechowych. Coraz więcej danych wskazuje jednak, że istotne znaczenie kliniczne ma również u osób dorosłych, zwłaszcza w populacji seniorów oraz u pacjentów z chorobami przewlekłymi, w tym układu sercowo-naczyniowego, oddechowego czy metabolicznego, a także u osób z obniżoną odpornością.
Z kolei Streptococcus pneumoniae pozostaje jednym z najważniejszych bakteryjnych patogenów układu oddechowego. Pneumokoki odpowiadają za szerokie spektrum chorób – od zapalenia zatok i ucha środkowego po zapalenie płuc oraz inwazyjną chorobę pneumokokową, obejmującą bakteriemię i zapalenie opon mózgowo-rdzeniowych. Istotną cechą tych bakterii jest duża różnorodność antygenowa – opisano ponad 100 ich serotypów. Szczególnym wyzwaniem klinicznym jest także narastająca wśród S. pneumoniae oporność na antybiotyki.
Interakcje pomiędzy wirusami i bakteriami uznawane są za jeden z kluczowych czynników wpływających na ciężkość przebiegu zakażeń dróg oddechowych. Infekcje wirusowe mogą sprzyjać wtórnym zakażeniom bakteryjnym poprzez uszkodzenie nabłonka oddechowego, zaburzenie odpowiedzi immunologicznej gospodarza czy zmiany w składzie mikrobioty dróg oddechowych. Z drugiej strony obecność bakterii kolonizujących drogi oddechowe może również wpływać na przebieg zakażeń wirusowych, modyfikując odpowiedź zapalną, dynamikę replikacji wirusa czy stopień uszkodzenia tkanek. Zrozumienie tych dwukierunkowych zależności ma kluczowe znaczenie dla strategii profilaktycznych. Dotyczy to także RSV i pneumokoków, które współdziałając mogą zwiększać ryzyko ciężkiego przebiegu zakażeń dolnych dróg oddechowych.
Jak RSV pomaga pneumokokom stwarzać zagrożenie?
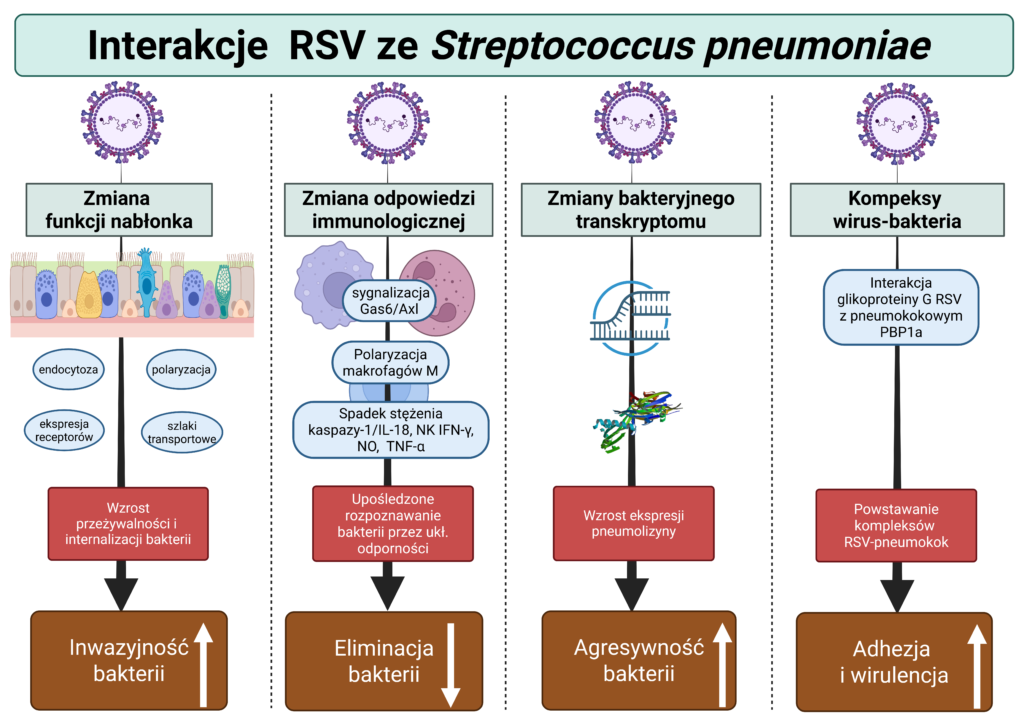
Jednym z podstawowych mechanizmów zwiększających ryzyko infekcji bakteryjnych jest wpływ RSV na strukturę i funkcję nabłonka oddechowego. Zakażenie wirusem prowadzi do zaburzenia integralności połączeń międzykomórkowych oraz przebudowy cytoszkieletu komórek wyściełających drogi oddechowe. W efekcie zwiększa się przepuszczalność bariery nabłonkowej, a także ekspresja receptorów adhezyjnych, do których mogą przyłączać się pneumokoki. Zmiany te nie tylko ułatwiają przyleganie bakterii do powierzchni komórek, lecz także sprzyjają ich internalizacji oraz przechodzeniu przez warstwę nabłonka do głębszych struktur dróg oddechowych. W praktyce oznacza to większe ryzyko przejścia od bezobjawowej kolonizacji do zakażenia inwazyjnego.
Odpowiedź układu odpornościowego na zakażenie RSV może paradoksalnie sprzyjać przeżywalności pneumokoków w drogach oddechowych. Wirus może zaburzać aktywność makrofagów oraz neutrofili – komórek kluczowych dla eliminacji bakterii w procesie fagocytozy. Jednocześnie dochodzi do zmian w profilu cytokin zapalnych oraz zaburzenia mechanizmów regulacyjnych odpowiedzi immunologicznej, co również sprzyja utrzymywaniu się bakterii w drogach oddechowych.
Bezpośrednie interakcje między RSV a pneumokokami mogą dodatkowo zwiększać patogenność bakterii. Wykazano, że glikoproteina G RSV może wiązać się z białkami powierzchniowymi pneumokoków, co prowadzi do zmian w ekspresji niektórych genów tych bakterii. W rezultacie zwiększa się produkcja m.in. pneumolizyny – toksyny odgrywającej kluczową rolę w uszkodzeniu tkanek, zaburzeniu funkcji komórek odpornościowych oraz ułatwianiu inwazji bakterii do krwiobiegu.
Badania eksperymentalne wskazują również na możliwość bezpośredniego tworzenia kompleksów wirus–bakteria. Takie struktury mogą zwiększać zdolność pneumokoków do przylegania do komórek nabłonka oraz nasilać ich wirulencję. W konsekwencji współzakażenie RSV i pneumokokami może prowadzić do bardziej nasilonego uszkodzenia tkanek i cięższego przebiegu klinicznego niż zakażenie wywołane przez jeden patogen.
Z klinicznego punktu widzenia współzakażenia – bądź następujące bezpośrednio po sobie infekcje RSV i S. pneumoniae – wiążą się z większym ryzykiem ciężkiego przebiegu choroby. U dzieci z zakażeniem RSV obecność pneumokoków w drogach oddechowych koreluje z wyższymi wskaźnikami ciężkości choroby, częstszymi hospitalizacjami oraz większym stopniem zajęcia dolnych dróg oddechowych.
Obserwacje u dorosłych wskazują natomiast, że zakażenie RSV, w przeciwieństwie do infekcji wywoływanych przez rinowirusy, wirusy paragrypy czy sezonowe koronawirusy, może nawet pięciokrotnie zwiększać ryzyko kolonizacji dróg oddechowych przez bakterie oraz sprzyjać zwiększeniu ich ładunku w górnych drogach oddechowych. Z jednej strony zwiększa to ryzyko progresji do bardziej inwazyjnej postaci choroby, z drugiej natomiast sprzyja transmisji patogenów w populacji.
Profilaktyka – wspólny cel dla dwóch patogenów
Dla lekarzy podstawowej opieki zdrowotnej świadomość tych interakcji ma istotne znaczenie praktyczne, zarówno w kontekście oceny ryzyka ciężkiego przebiegu zakażeń, jak i planowania działań profilaktycznych u pacjentów z grup zwiększonego ryzyka. Coraz więcej danych wskazuje bowiem, że o profilaktyce zakażeń pneumokokowych można myśleć już na etapie zapobiegania zakażeniom RSV – nie zapominając oczywiście o szczepieniach ukierunkowanych przeciwko pneumokokom.
W ostatnich latach pojawiły się nowe narzędzia profilaktyczne przeciw RSV dostępne również w Polsce. U niemowląt możliwe jest zastosowanie długodziałających przeciwciał monoklonalnych, czyli preparatu o nazwie nirsewimab. Zapewnia on bierną immunizację poprzez bezpośrednie dostarczenie przeciwciał neutralizujących wirusa i może chronić dziecko przez cały sezon epidemiczny RSV po podaniu pojedynczej dawki. Jest to istotna przewaga nad wcześniejszymi rozwiązaniami wymagającymi wielokrotnych podań w trakcie sezonu. Obecnie preparat nie jest jeszcze refundowany w Polsce, jednak stanowi ważne narzędzie profilaktyczne, szczególnie u najmłodszych dzieci w pierwszym sezonie ekspozycji na RSV.
Z kolei profilaktyka RSV wśród dorosłych opiera się o szczepionki, które są w Polsce objęte refundacją w wysokości 100% dla osób powyżej 65. roku życia oraz w wysokości 50% dla pacjentów w wieku 60–64 lata. Młodsi dorośli mogą korzystać z tych szczepień w ramach profilaktyki komercyjnej. Dodatkowo, nieadiuwantowana szczepionka biwalentna jest w pełni refundowana kobietom w ciąży, co przyczynia się do lepszej ochrony ich przyszłych dzieci w pierwszych miesiącach po urodzeniu poprzez przezłożyskowy transfer przeciwciał.
Równolegle funkcjonuje profilaktyka skierowana przeciw pneumokokom. W Polsce szczepienia przeciwko S. pneumoniae wśród dzieci są obowiązkowe. Dzięki temu znacząco ograniczono częstość ciężkich zakażeń pneumokokowych w najmłodszych grupach wiekowych. Z kolei osobom w wieku 65+ szczepienia przeciw pneumokokom są refundowane. W praktyce klinicznej oznacza to, że lekarz dysponuje dziś realnymi narzędziami ograniczania ryzyka zarówno zakażeń RSV, jak i chorób pneumokokowych. Wykorzystanie tych możliwości – szczególnie u niemowląt, osób starszych oraz pacjentów z chorobami przewlekłymi – może przyczynić się do zmniejszenia liczby ciężkich zakażeń dróg oddechowych, hospitalizacji oraz powikłań.
Taka profilaktyka może mieć również znaczenie w kontekście narastającego problemu antybiotykoodporności wśród pneumokoków. Szacuje się, że w Wielkiej Brytanii sam RSV – poprzez sprzyjanie wtórnym zakażeniom bakteryjnym – odpowiada za około 2% całkowitego zużycia antybiotyków w populacji. Im mniej zakażeń RSV, tym potencjalnie mniejsza liczba sytuacji wymagających antybiotykoterapii, a tym samym mniejsza presja selekcyjna sprzyjająca pojawianiu się szczepów opornych. Problem ten jest szczególnie istotny w przypadku pneumokoków, wśród których coraz częściej obserwuje się szczepy wielolekooporne, zwłaszcza w przypadku serotypów 19F, 23F, 15A czy 6B. Dodatkowo ponad 15% pacjentów hospitalizowanych z powodu RSV doświadcza nadkażenia bakteryjnego, które pogarsza ich rokowanie. W tym kontekście nie dziwi, że skuteczna profilaktyka RSV może pośrednio przyczyniać się do ograniczenia problemu antybiotykooporności. Tego typu efekt zaobserwowano w badaniach, które wykazały, że niemowlęta, których matki zostały zaszczepione przeciw RSV w czasie ciąży, wymagały nawet o połowę rzadziej antybiotykoterapii z powodu infekcji dróg oddechowych. A przecież stosowanie antybiotyków na wczesnym etapie życia może niekorzystnie wpływać na rozwijający się mikrobiom dziecka, a w konsekwencji na dojrzewanie i regulację układu odpornościowego.
Wspólny front przeciw zakażeniom
Przykład RSV i pneumokoków dowodzi, że pojedynczy patogen układu oddechowego rzadko działa w izolacji. Skuteczna profilaktyka jednego z nich może przynosić szersze korzyści zdrowotne – ograniczając ciężkość chorób wywoływanych przez inne drobnoustroje. W praktyce oznacza to, że działania profilaktyczne ukierunkowane na RSV mogą stać się jednym z elementów strategii zmniejszania obciążenia chorobami pneumokokowymi i problemem antybiotykooporności.
Prof. dr hab. n.med i n. o zdr. Piotr Rzymski